
Ricondizionamento dei dispositivi medici monouso (ai sensi del Regolamento MD)
ID 13138 | Rev. 00 del 18.03.2020 / Documento completo allegato
Il Regolamento (UE) 2017/745, prevede all’Art. 17 (Dispositivi monouso e loro ricondizionamento), le prescrizioni per il ricondizionamento e l'ulteriore utilizzo dei dispositivi monouso. Con il Regolamento di esecuzione (UE) 2020/1207 (GU L 273/3 del 20.08.2020), sono state stabilite le Specifiche Comuni (SC) in esecuzione dell’Art. 17 p. 3 del Regolamento (UE) 2017/745 che consente la deroga al p. 2 relativa alla persona fisica o giuridica che ricondiziona un dispositivo monouso che potrà non assumere gli obblighi imposti ai fabbricanti dal Regolamento (UE) 2017/745.
Le istituzioni sanitarie che ricondizionano dispositivi monouso, dovranno conformarti all'articolo 17 del Regolamento (UE) 2017/745. Il regolamento aggiunge condizioni rigorose per il ricondizionamento dei dispositivi medici monouso e pone la piena responsabilità del prodotto sul ricondizionatore. Inoltre, il ricondizionamento può avvenire solo se autorizzato dalla legislazione nazionale e conformemente alle disposizioni del MDR. Alcuni paesi dell'UE potrebbero avere disposizioni più severe o addirittura vietare il ricondizionamento.
Pubblicato nella GU L 273/3 del 20.08.2020 il Regolamento di esecuzione (UE) 2020/1207 che stabilisce le norme per l’applicazione dell’articolo 17, paragrafo 3, del Regolamento (UE) 2017/745, qualora il diritto nazionale autorizzi il ricondizionamento dei dispositivi monouso e uno Stato membro abbia deciso di non applicare tutte le norme relative agli obblighi dei fabbricanti previste in tale regolamento in relazione ai dispositivi monouso ricondizionati e utilizzati all’interno di un’istituzione sanitaria.
Il regolamento stabilisce inoltre le norme applicabili nel caso in cui uno Stato membro abbia deciso di applicare l’articolo 17, paragrafo 3, del Regolamento (UE) 2017/745 anche per quanto riguarda i dispositivi monouso ricondizionati da un ricondizionatore esterno. Esso si applica a decorrere dal 26 maggio 2021.
...
Regolamento (UE) 2017/745
Articolo 17. Dispositivi monouso e loro ricondizionamento
1. Il ricondizionamento e l'ulteriore utilizzo dei dispositivi monouso è autorizzato solo se consentito dal diritto nazionale e solo a norma del presente articolo.
2. Una persona fisica o giuridica che ricondiziona un dispositivo monouso per renderlo adatto a un ulteriore utilizzo nell'Unione è considerata il fabbricante del dispositivo ricondizionato e assume gli obblighi imposti ai fabbricanti dal presente regolamento, ivi compresi gli obblighi connessi alla tracciabilità del dispositivo ricondizionato, conformemente al capo III del presente regolamento. Il ricondizionatore del dispositivo è considerato un produttore ai fini dell'articolo 3, paragrafo 1, della direttiva 85/374/CEE.
3. In deroga al paragrafo 2, gli Stati membri possono decidere di non applicare tutte le norme relative agli obblighi dei fabbricanti previste nel presente regolamento in relazione ai dispositivi monouso ricondizionati e utilizzati all'interno di un'istituzione sanitaria, purché garantiscano che:
a) la sicurezza e le prestazioni del dispositivo ricondizionato sono equivalenti a quelle del dispositivo d'origine e che le prescrizioni di cui all'articolo 5, paragrafo 5, lettere a), b), d), e), f), g) e h) sono rispettate;
b) il ricondizionamento è effettuato a norma delle SC (*) che precisano le prescrizioni applicabili:
- alla gestione del rischio, comprese l'analisi della fabbricazione e i materiali, le proprietà relative del dispositivo (ingegneria inversa) e le procedure necessarie a individuare le modifiche nella progettazione del dispositivo originale e la sua prevista applicazione dopo il ricondizionamento,
- alla convalida delle procedure per l'intero processo, tra cui le fasi relative alla pulizia,
- al rilascio del prodotto e ai test sulla prestazione,
- al sistema di gestione della qualità,
- alla segnalazione di incidenti relativi a dispositivi sottoposti a ricondizionamento, e
- alla tracciabilità dei dispositivi ricondizionati. Gli Stati membri incoraggiano le istituzioni sanitarie, e possono obbligarle, a fornire ai pazienti informazioni sull'uso dei dispositivi ricondizionati all'interno dell'istituzione sanitaria e, se del caso, qualsiasi altra informazione pertinente sui dispositivi ricondizionati con cui tali pazienti sono trattati. Gli Stati membri informano la Commissione e gli altri Stati membri delle disposizioni nazionali adottate in virtù del presente paragrafo e dei motivi che ne giustificano l'adozione. La Commissione mette tali informazioni a disposizione del pubblico.
4. Gli Stati membri possono scegliere di applicare le disposizioni di cui al paragrafo 3 anche ai dispositivi monouso ricondizionati da un soggetto esterno su richiesta di un'istituzione sanitaria, purché il dispositivo ricondizionato nella sua totalità sia rinviato alla medesima istituzione sanitaria e il soggetto esterno soddisfi le prescrizioni di cui al paragrafo 3, lettere a) e b).
5. La Commissione adotta, ai sensi dell'articolo 9, paragrafo 1, le necessarie SC di cui al paragrafo 3, lettera b) entro il 26 maggio 2021. Tali SC sono coerenti con i più recenti dati scientifici e riguardano l'applicazione dei requisiti generali di sicurezza e prestazione di cui al presente regolamento. Se le SC non sono adottate entro il 26 maggio 2021, il ricondizionamento è effettuato secondo le norme armonizzate pertinenti e le disposizioni nazionali che garantiscono il rispetto delle prescrizioni previste al paragrafo 3, lettera b). Il rispetto delle SC o, in assenza di queste, delle norme armonizzate pertinenti e delle disposizioni nazionali è certificato da un organismo notificato.
6. Possono essere ricondizionati solo i dispositivi monouso che sono stati immessi sul mercato conformemente al presente regolamento o, prima del 26 maggio 2021, conformemente alla direttiva 93/42/CEE.
7. Il ricondizionamento di dispositivi monouso può essere effettuato solo se considerato sicuro in base ai più recenti dati scientifici.
8. Il nome e l'indirizzo della persona fisica o giuridica di cui al paragrafo 2 e le altre informazioni pertinenti di cui all'allegato I, punto 23, figurano sull'etichetta e, se del caso, nelle istruzioni per l'uso del dispositivo ricondizionato. Il nome e l'indirizzo del fabbricante del dispositivo monouso iniziale non figurano più sull'etichetta, ma sono indicati nelle istruzioni per l'uso del dispositivo ricondizionato.
9. Uno Stato membro che consente il ricondizionamento di dispositivi monouso può mantenere o introdurre disposizioni nazionali più rigorose di quelle previste dal presente regolamento, che limitino o vietino nel proprio territorio:
a) il ricondizionamento di dispositivi monouso e il trasferimento di dispositivi monouso in un altro Stato membro o in un paese terzo per esservi ricondizionati;
b) la messa a disposizione o l'ulteriore utilizzo di dispositivi monouso ricondizionati. Gli Stati membri informano la Commissione e gli altri Stati membri di tali disposizioni nazionali. La Commissione rende disponibile al pubblico tali informazioni.
10. Entro il 27 maggio 2024 la Commissione redige una relazione sul funzionamento del presente articolo e la presenta al Parlamento europeo e al Consiglio. Sulla base di tale relazione, la Commissione, se del caso, presenta proposte di modifica del presente regolamento.
(*) (SC) Specifiche Comuni
Regolamento (UE) 2017/745
71) «specifiche comuni» (SC): una serie di requisiti tecnici e/o clinici, diversi da una norma, che consentono di rispettare gli obblighi giuridici applicabili a un dispositivo, a un processo o a un sistema.
Le Specifiche Comuni (SC) sono state pubblicate con il Regolamento di esecuzione (UE) 2020/1207 della Commissione del 19 agosto 2020 recante modalità di applicazione del regolamento (UE) 2017/745 del Parlamento europeo e del Consiglio per quanto riguarda le specifiche comuni per il ricondizionamento dei dispositivi monouso (GU L 273/3 del 23.08.2020).
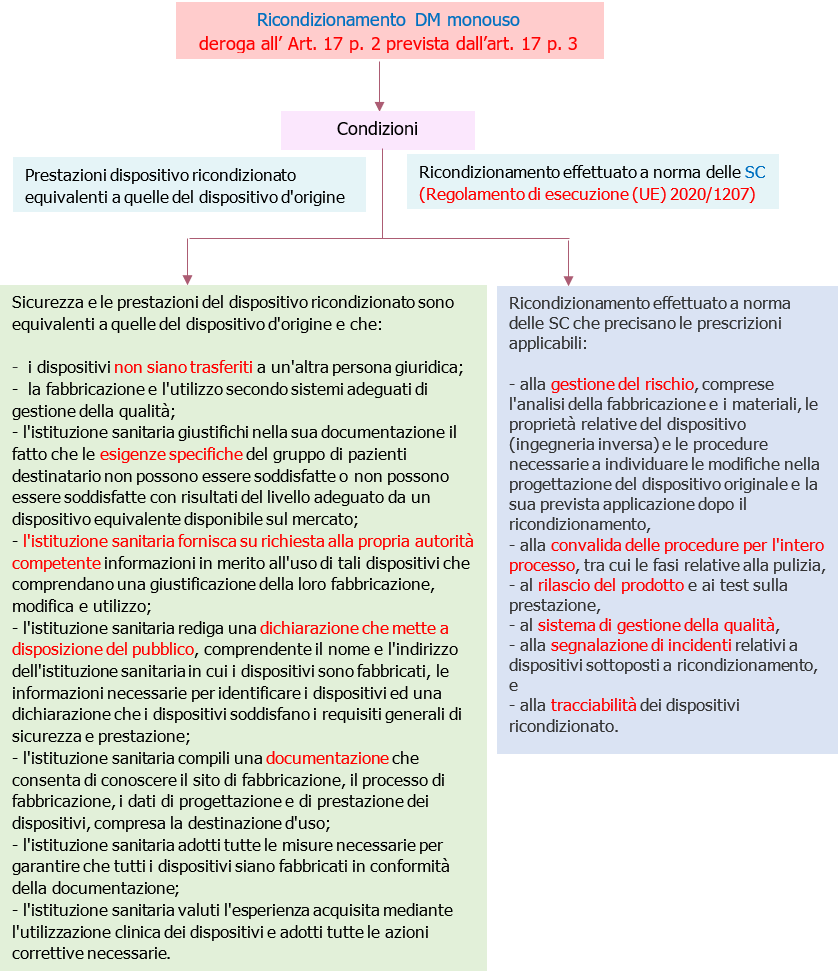
Figura 1 - Ricondizionamento DM monouso (Deroga Art. 17 p. 3)
...
Regolamento di esecuzione (UE) 2020/1207
della Commissione del 19 agosto 2020 recante modalità di applicazione del regolamento (UE) 2017/745 del Parlamento europeo e del Consiglio per quanto riguarda le specifiche comuni per il ricondizionamento dei dispositivi monouso (GU L 273/3 del 23.08.2020).
Regolamento di esecuzione (UE) 2020/1207
Articolo 3 Ricondizionatori esterni contraenti
1. Se il ricondizionamento è effettuato da un ricondizionatore esterno, l’istituzione sanitaria e il ricondizionatore esterno concludono un contratto scritto.
2. Il contratto comprende i seguenti elementi:
a) l’attribuzione dei compiti, degli obblighi e delle responsabilità delle due parti;
b) le disposizioni per il passaggio da un ricondizionatore esterno a un altro e le responsabilità del ricondizionatore esterno che è parte del contratto;
c) i requisiti relativi alla qualifica e alle competenze del personale che partecipa alle attività di ricondizionamento;
d) gli obblighi relativi al ricondizionamento, alla raccolta di informazioni riguardanti i dispositivi ricondizionati e allo scambio di informazioni tra l’istituzione sanitaria e il ricondizionatore esterno;
e) l’obbligo di garantire la compatibilità dei sistemi di gestione della qualità delle parti, di cui all’articolo 21;
f) la procedura per il monitoraggio della qualità del ricondizionamento effettuato dal ricondizionatore esterno mediante audit in loco.
Articolo 4 Personale, locali e attrezzature
1. Il ricondizionatore provvede affinché il personale addetto al ricondizionamento:
a) sia sufficiente a garantire la qualità del ricondizionamento;
b) possieda le conoscenze specifiche pertinenti e una formazione professionale sufficiente in considerazione delle fasi di ricondizionamento applicate;
c) abbia compiti e responsabilità chiaramente definiti per iscritto.
2. Il ricondizionatore designa una o più persone responsabili del ricondizionamento.
3. La persona responsabile del ricondizionamento soddisfa i seguenti criteri:
a) possiede esperienza e qualifiche sufficienti nel campo del ricondizionamento;
b) ha ricevuto una formazione in materia di segnalazione di incidenti e di analisi critica conformemente all’articolo 23, paragrafo 8.
La persona responsabile del ricondizionamento è permanentemente e continuamente a disposizione del ricondizionatore durante l’orario di lavoro di quest’ultimo. La persona responsabile del ricondizionamento è anche responsabile dell’elaborazione e della gestione della documentazione tecnica di cui all’articolo 9 e del sistema di gestione della qualità di cui all’articolo 21.
4. I locali in cui avviene il ricondizionamento e le attrezzature utilizzate sono adattati al tipo di dispositivi monouso da sottoporre a ricondizionamento, alle fasi del ciclo di ricondizionamento e al numero di fasi di ricondizionamento.
5. Le superfici dei locali, l’aria ambiente (temperatura, umidità, particelle sospese vitali e non vitali), l’acqua e gli altri gas e fluidi sono controllati e monitorati periodicamente per verificare che la qualità microbiologica e fisica sia adeguata al ricondizionamento.
6. Le attrezzature sono periodicamente sottoposte, secondo le istruzioni del fabbricante, a manutenzione, controlli delle prestazioni e calibrazioni generalmente riconosciuti come i più avanzati. Le attrezzature sono convalidate e, ove applicabile, periodicamente riconvalidate, al fine di stabilire se siano adatte alla destinazione d’uso.
7. Il ricondizionatore descrive nella documentazione tecnica di cui all’articolo 9, paragrafo 1, i tipi di dispositivi monouso per i quali ha deciso di essere in grado di effettuare il ricondizionamento e la motivazione di tale decisione. Il ricondizionatore rende disponibile al pubblico l’elenco dei dispositivi che è in grado di ricondizionare.
8. Se decide che non è più in grado di ricondizionare determinati tipi di dispositivi monouso, il ricondizionatore descrive i motivi di tale decisione nella documentazione tecnica di cui all’articolo 9, paragrafo 1. L’elenco di cui al paragrafo 7 del presente articolo è aggiornato di conseguenza.
Articolo 5 Valutazione preliminare dell’idoneità di un dispositivo monouso al ricondizionamento
1. Prima di decidere di iniziare a ricondizionare un dispositivo monouso, o di chiedere di farlo a un ricondizionatore esterno, l’istituzione sanitaria valuta se il dispositivo monouso sia adatto al ricondizionamento.
2. Ai fini del paragrafo 1, l’istituzione sanitaria valuta se la sicurezza e le prestazioni del dispositivo monouso una volta ricondizionato saranno equivalenti a quelle del dispositivo monouso d’origine.
3. Nel valutare l’idoneità di un dispositivo monouso al ricondizionamento, l’istituzione sanitaria, ove applicabile:
a) verifica che il dispositivo monouso rechi la marcatura CE;
b) verifica che il dispositivo monouso non sia stato ritirato dal mercato e che il suo certificato di conformità non sia stato sospeso, ritirato o sottoposto a limitazioni;
c) verifica se l’utilizzo del dispositivo monouso sia stato sottoposto a limitazioni per motivi di sicurezza, secondo quanto indicato negli avvisi di sicurezza;
d) effettua un’analisi delle proprietà del dispositivo monouso, tenendo conto di tutta la documentazione e di tutte le informazioni disponibili sul dispositivo monouso, per garantire una comprensione e una conoscenza sufficienti in materia di progettazione, proprietà di fabbricazione, caratteristiche dei materiali, proprietà funzionali e altri fattori di rischio connessi al ricondizionamento del dispositivo monouso, compreso l’uso precedente.
Ove applicabile, nell’effettuare una valutazione a norma del primo comma, l’istituzione sanitaria consulta un ricondizionatore esterno e si avvale del suo sostegno operativo conformemente al contratto di cui all’articolo 3.
Ai fini delle lettere b) e c), l’istituzione sanitaria verifica le informazioni contenute nella banca dati europea dei dispositivi medici (Eudamed). Fino a quando Eudamed non sarà pienamente operativa, l’istituzione sanitaria verifica le informazioni conformemente alle disposizioni sullo scambio di informazioni di cui all’articolo 123, paragrafo 3, lettera d), del regolamento (UE) 2017/745.
Qualora le informazioni non possano essere ottenute conformemente al terzo comma, l’istituzione sanitaria verifica le informazioni sul sito web del fabbricante o del suo mandatario.
Ai fini della lettera d), l’istituzione sanitaria riesamina le informazioni di cui all’allegato I, capo III, punto 23.4, lettera p), del regolamento (UE) 2017/745 e qualsiasi altra documentazione e informazione pertinente di pubblico dominio.
4. La decisione dell’istituzione sanitaria in merito all’idoneità di un dispositivo monouso al ricondizionamento è basata su un parere positivo scritto fornito dalla persona responsabile del ricondizionamento. Il dispositivo monouso non viene ricondizionato se la persona responsabile del ricondizionamento ha espresso un parere negativo sull’idoneità del dispositivo monouso al ricondizionamento.
Articolo 6 Destinazione d’uso originaria e monitoraggio delle modifiche apportate dal fabbricante del dispositivo monouso d’origine
1. Il ricondizionatore non modifica la destinazione d’uso originaria del dispositivo monouso quale indicata nelle istruzioni per l’uso.
2. Il ricondizionatore stabilisce un processo di monitoraggio al fine di verificare:
a)
che il dispositivo monouso non sia ritirato dal mercato;
b) che il certificato di conformità del dispositivo monouso non sia stato sospeso, ritirato o sottoposto a limitazioni;
c) che l’utilizzo del dispositivo monouso non sia sottoposto a limitazioni per motivi di sicurezza sulla base delle informazioni di cui all’articolo 5, paragrafo 3, lettere b) e c).
Il ricondizionatore individua inoltre qualsiasi modifica apportata dal fabbricante a componenti, materiali, destinazione d’uso o specifiche del dispositivo monouso che possa incidere sul ricondizionamento. Il ricondizionatore valuta l’importanza di tali modifiche per l’adeguatezza del ricondizionamento. Se una modifica incide negativamente sul dispositivo monouso ricondizionato, il ricondizionamento è interrotto o il processo di ricondizionamento è modificato per adattarlo alla modifica apportata al dispositivo monouso.
Articolo 7 Determinazione del ciclo di ricondizionamento
1. Le istituzioni sanitarie che ricondizionano dispositivi monouso stabiliscono, se applicabile insieme ai ricondizionatori esterni, il ciclo di ricondizionamento del dispositivo monouso da sottoporre a ricondizionamento.
2. Il ciclo di ricondizionamento è stabilito in base alla documentazione e alle informazioni raccolte conformemente all’articolo 5 e ai risultati di una valutazione tecnica che comprende, ove opportuno, test fisici, elettrici, chimici, biologici e microbiologici, e ingegneria inversa. Il ciclo di ricondizionamento non modifica la destinazione d’uso del dispositivo monouso, tiene conto delle conoscenze scientifiche e tecniche e, se applicabile, del metodo originale di sterilizzazione e delle norme pertinenti.
3. Il ciclo di ricondizionamento è stabilito per iscritto ed è convalidato dall’istituzione sanitaria che ricondiziona i dispositivi monouso, se applicabile insieme ai ricondizionatori esterni. Il ciclo di ricondizionamento descrive ogni fase del ricondizionamento. Per ciascuna fase è stabilita la procedura pertinente e ogni fase è convalidata. La convalida delle fasi di ricondizionamento consiste nell’installazione e nelle qualifiche del funzionamento e delle prestazioni.
4. La convalida garantisce che le prestazioni e la sicurezza del dispositivo monouso rimangano equivalenti a quelle del dispositivo monouso d’origine dopo ogni ciclo di ricondizionamento e fino al numero massimo consentito di cicli di ricondizionamento.
5. Il ciclo di ricondizionamento è monitorato mediante periodici test di routine e controlli della contaminazione, monitoraggi fisici, elettrici, chimici e biologici e verifiche dei parametri di processo e della calibrazione.
6. Il dispositivo monouso ricondizionato è rilasciato dopo che è stato confermato che le fasi di pulizia, disinfezione e sterilizzazione e i test pertinenti secondo i casi assicurano che il ciclo di ricondizionamento è stato completato conformemente alle prescrizioni applicabili a tale ciclo.
Articolo 8 Numero massimo di cicli di ricondizionamento
1. Ciascun ricondizionamento conforme all’articolo 11 è conteggiato come un unico ciclo di ricondizionamento. Ogni ciclo di ricondizionamento di un dispositivo monouso è conteggiato per determinare il numero massimo di cicli di ricondizionamento, anche qualora un dispositivo monouso non sia stato riutilizzato su un paziente in seguito al ricondizionamento.
2. L’istituzione sanitaria, se applicabile insieme al ricondizionatore esterno, stabilisce il numero massimo di cicli di ricondizionamento che possono essere applicati al dispositivo monouso ricondizionato durante i quali le prestazioni e la sicurezza di tale dispositivo rimangono equivalenti a quelle del dispositivo monouso d’origine.
3. Una volta raggiunto il numero massimo di cicli di ricondizionamento, il dispositivo monouso ricondizionato è smaltito.
Articolo 9 Documentazione tecnica
1. Il ricondizionatore dispone di una documentazione tecnica sulle sue attività di ricondizionamento che comprende:
a) le procedure di controllo e monitoraggio periodico dei locali e delle attrezzature di cui all’articolo 4, paragrafi 5 e 6;
b) qualsiasi decisione relativa al fatto di essere in grado o meno di ricondizionare un tipo di dispositivo monouso.
2. Il ricondizionatore dispone anche di una documentazione tecnica specifica per ciascun modello di dispositivo monouso, fabbricato dallo stesso fabbricante, quale identificato dal suo identificativo del dispositivo nel sistema di identificazione unica del dispositivo («UDI-DI»). La documentazione tecnica comprende:
a) i risultati della determinazione del ciclo e delle procedure di ricondizionamento di cui all’articolo 7;
b) le azioni da intraprendere nel caso in cui una o più fasi del ciclo di ricondizionamento non siano state eseguite.
3. La documentazione tecnica specifica per ciascun modello di dispositivo monouso fabbricato dallo stesso fabbricante, quale identificato dal suo UDI-DI, conservata dalle istituzioni sanitarie comprende altresì:
a) i risultati della valutazione dell’idoneità del dispositivo monouso al ricondizionamento di cui all’articolo 5 e i dati e le informazioni utilizzati per stabilire che la sicurezza e le prestazioni del dispositivo ricondizionato saranno equivalenti a quelle del dispositivo monouso d’origine;
b) i risultati del processo di monitoraggio di cui all’articolo 6;
c) la descrizione del sistema di tracciabilità del dispositivo monouso dal primo utilizzo fino al suo ultimo riutilizzo;
d) la descrizione del sistema di segnalazione di incidenti gravi conformemente all’articolo 23;
e) la descrizione del sistema di identificazione e di smaltimento del dispositivo monouso in caso di mancata conformità ad aspetti di funzionalità, prestazioni o sicurezza prima o durante il riutilizzo.
4. La documentazione tecnica è conservata per 10 anni dopo l’ultimo riutilizzo del dispositivo monouso.
CAPO III PROCEDURE E FASI DEL CICLO DI RICONDIZIONAMENTO
Articolo 10 Stabilimento delle procedure
1. Prima di iniziare il ricondizionamento, il ricondizionatore effettua un controllo visivo dei dispositivi monouso per individuare eventuali danni. Verifica che i pezzi mobili si muovano correttamente. Qualora il dispositivo monouso debba essere sottoposto a manutenzione o tarato per poter funzionare come specificato nelle istruzioni per l’uso, la manutenzione è effettuata conformemente alla procedura stabilita. Il ricondizionatore provvede allo smaltimento dei dispositivi monouso danneggiati o mal funzionanti.
2. Il ricondizionatore stabilisce una procedura convalidata di decontaminazione adattata alle proprietà e alle caratteristiche del dispositivo monouso e ai rischi connessi al suo utilizzo.
3. La preparazione per il ricondizionamento non compromette lo stato igienico e la funzionalità del dispositivo decontaminato. In caso di ritardo superiore a un termine stabilito nella procedura prima della pulizia e della disinfezione o sterilizzazione, il dispositivo monouso è sottoposto a un’adeguata pulizia preliminare e a immagazzinamento intermedio. I dispositivi monouso sono trasportati nei locali di ricondizionamento in appositi contenitori chiusi e identificati, secondo le condizioni stabilite in una procedura.
4. I requisiti necessari in termini di proprietà microbiologiche e chimiche dell’acqua, delle sostanze chimiche e di altri prodotti utilizzati nel ricondizionamento sono indicati nelle procedure relative a ciascun ciclo specifico.
5. Nella scelta delle procedure di pulizia, disinfezione e sterilizzazione, è data priorità a procedure automatizzate convalidate che ne garantiscano la riproducibilità. La disinfezione garantisce adeguati effetti battericidi (anche sui micobatteri), fungicidi e virucidi, e l’efficacia della disinfezione è verificata periodicamente su campioni.
6. Le soluzioni di pulizia e disinfezione e, se applicabile, l’agente sterilizzante sono rimossi con un metodo convalidato descritto in una procedura.
7. La sterilizzazione con calore umido (sterilizzazione a vapore) è utilizzata nei casi in cui è appropriata. Altri metodi convalidati possono tuttavia essere scelti in base alle proprietà e alle caratteristiche del dispositivo monouso da sottoporre a ricondizionamento.
8. Il monitoraggio dei cicli di sterilizzazione e il rilascio dei dispositivi monouso sterilizzati si basano sul raggiungimento di parametri di sterilizzazione entro i limiti di tolleranza stabiliti e convalidati descritti in una procedura. Se non è possibile misurare tutti i parametri di sterilizzazione pertinenti, tali misurazioni fisiche sono completate utilizzando idonei indicatori biologici che forniscano ulteriori garanzie che non si sono verificate variazioni non rilevate rispetto al ciclo convalidato.
9. Il sistema di confezionamento è adeguato al contenuto, convalidato secondo le norme pertinenti e il metodo di sterilizzazione utilizzato, se applicabile, convalidato per le proprietà del dispositivo monouso ricondizionato e per l’immagazzinamento e il trasporto previsti. Il confezionamento permette la sterilizzazione e garantisce la sterilità durante la durata di vita dichiarata e fino all’utilizzo, in condizioni adeguate di immagazzinamento e trasporto. Se durante il ricondizionamento è rilevato un problema relativo alla funzionalità, alle prestazioni o alla sicurezza del dispositivo monouso, il problema è affrontato e il dispositivo monouso è riparato, se possibile, o smaltito se la riparazione non è possibile. La causa del problema è indagata per verificare che il ciclo continui ad essere efficace. Se non raggiunge più l’obiettivo, il ciclo viene modificato o il ricondizionamento è interrotto per tale dispositivo monouso specifico. Se una delle fasi del ricondizionamento non soddisfa i requisiti stabiliti nelle procedure per un dato dispositivo monouso, tale dispositivo monouso non è rilasciato per il riutilizzo.
Articolo 11 Fasi del ciclo di ricondizionamento
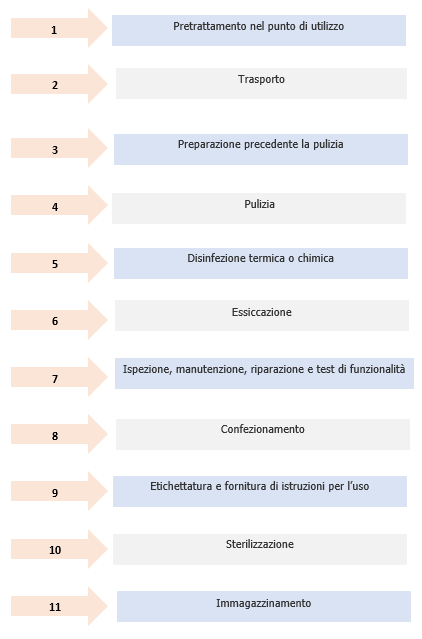
Il ciclo di ricondizionamento comprende le seguenti fasi, se applicabili al dispositivo in questione:
a) pretrattamento nel punto di utilizzo;
b) trasporto, comprese procedure per il trasporto sicuro di materiali pericolosi;
c) preparazione precedente la pulizia;
d) pulizia;
e) disinfezione termica o chimica;
f) essiccazione;
g) ispezione, manutenzione, riparazione e test di funzionalità;
h) confezionamento;
i) etichettatura e fornitura di istruzioni per l’uso;
j) sterilizzazione;
k) immagazzinamento.
Figura 2 - Fasi del ciclo di ricondizionamento
...
segue in allegato
Certifico Srl - IT | Rev. 00 2021
©Copia Autorizzata Abbonati
Collegati
Allegati
|
Descrizione |
Lingua |
Dimensioni |
Downloads |
 |
|
IT |
267 kB |
57 |



































