Prevenzione delle atmosfere di gas potenzialmente esplosive: i limiti LEL / UEL - Note 2023
| Appunti Prevenzione Incendi | |||||||||
| 02 Luglio 2025 | |||||||||
| Salve Visitatore | |||||||||
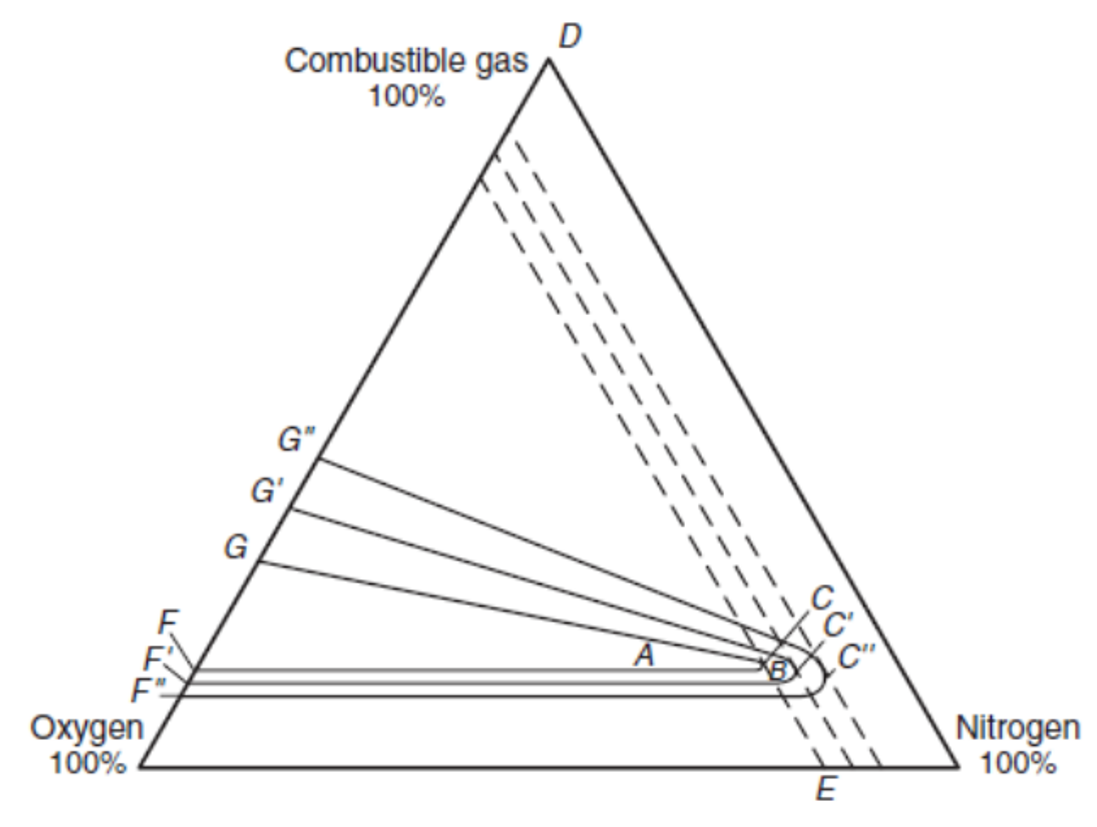
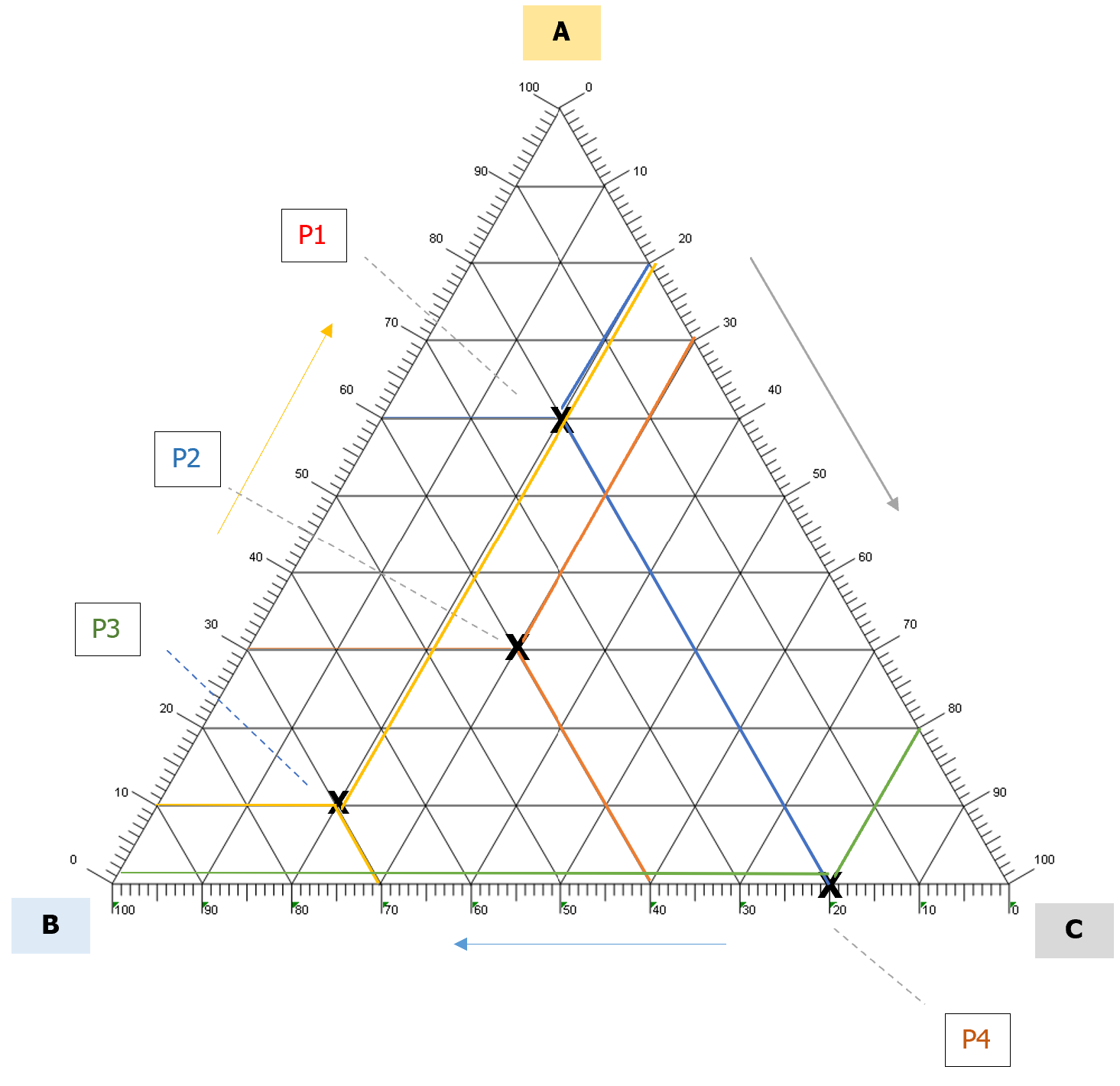
Prevenzione atmosfere gas potenzialmente esplosive: limiti LEL/UEL ID 20844 | 03.12.2023 / Documento completo in allegato NB: Il Documenti illustra, in termini tecnico-divulgativi, i limiti di esplosività LEL / EUL e parametri correlati MIE, LOC di un gas o dei vapori di un liquido in aria con esempi grafici. Note sull'intertizzazione di tali atmosfere. I limiti di esplosione (o limiti di esplosività) di un gas o dei vapori di un liquido sono dei limiti che definiscono l'intervallo di concentrazione entro cui, se la miscela aria-vapore o gas infiammabile è opportunamente innescata (ad esempio da una scintilla), si verifica l'accensione della miscela. Questa combustione può essere una detonazione o solamente una "fiammata" (deflagrazione), in funzione di numerosi fattori (concentrazione di combustibile in primis, tipo di recipiente). Il limite di esplosione viene considerato in un range che va da un minimo (L.I.E.= Limite inferiore di esplosività) ad un massimo (L.S.E.= Limite superiore di esplosività) di percentuale di combustibile in aria (o più raramente in altri comburenti); in inglese lower explosive limit (LEL), e upper explosive limit (UEL). Caratteristiche di innesco che individuano la minima e la massima energia di innesco del gas/vapori di liquido infiammabili Per ogni gas/vapori di liquido infiammabili è possibile tracciare una curva, come quella illustrata a seguire, che indica la caratteristica di innesco, dalla quale si determina la minima energia di innesco, chiamata M.I.E. (Minimum Ignition Energy), al di sotto della quale è impossibile l’innesco della miscela. Figura 1 - LEL - UEL / MIE L.E.L. (Lower Explosive Limit) U.E.L. (Upper Explosive Limit) M.I.E. (Minimum Ignition Energy) Ogni gas/vapori di liquido infiammabili ha un limite di concentrazione al di sotto del quale non può essere accesa quando viene miscelata con aria, in quanto non è presente abbastanza carburante. Il limite LEL è una proprietà empirica incalcolabile delle sostanze infiammabili, che è determinata sulla base di specifiche norme e che - con poche eccezioni - è compresa nell’intervallo tra 0,5 e 15% vol. Gas e vapori infiammabili possono essere attivati in specifiche condizioni atmosferiche - da una fonte di innesco con energia di accensione e/o temperatura abbastanza elevata in combinazione con concentrazioni di ossigeno nell’aria altrettanto elevate. Queste concentrazioni sono indicate, appunto come limite inferiore di esplosività (limite LEL). In altre parole, l’accensione può avvenire solo se sono soddisfatte tre condizioni: 1. Una concentrazione di gas o vapore infiammabile al di sopra del limite LEL. Lo stesso vale in senso inverso: se una qualsiasi di queste tre condizioni non viene soddisfatta, non vi sarà alcun modo per cui l’accensione o l’esplosione possa verificarsi. Misure di protezione Le misure di protezione contro le esplosioni possono quindi essere: Il modo più sicuro per limitare le concentrazioni è naturalmente quello di evitare completamente l’uso di gas/vapori infiammabili. Tuttavia raramente questo è possibile. Di conseguenza, per limitare le concentrazioni vengono utilizzate apparecchiature per la rilevazione del gas, mentre, nei processi che si svolgono in ambienti chiusi, di fatto viene permesso alle concentrazioni di raggiungere valori ben al di sopra del limite LEL, e il livello di ossigeno viene ridotto in misura tale che nessuna miscela infiammabile si possa formare (inertizzazione). Se tali misure fossero insufficienti, o non pienamente adeguate, in definitiva dovrebbero essere utilizzati solo tipi di apparecchiature operative protette contro l’accensione (standardizzate), per garantire che le apparecchiature non diventino una fonte di accensione in caso di perdite di gas. Soglie di allarme Se il limite LEL della concentrazione inizia ad aumentare, non appena raggiunge l’intervallo di allarme 1 vengono attivate delle contromisure. Se tali misure hanno successo la concentrazione diminuisce (curva blu). Tuttavia, se le misure non hanno successo, la concentrazione continua a salire (curva rossa). Una volta raggiunto il secondo intervallo di allarme 2, vengono attivate le misure di emergenza. Gli impianti industriali correttamente progettati raggiungono l’intervallo di allarme 2 solo in casi molto rari, se non mai. Figura 2 - Soglie intervalli di allarme Scale LEL Minore sarà il limite LEL e più pericolosa sarà la sostanza, poiché sarà più facile la formazione di concentrazioni infiammabili. Per esempio, il limite LEL dell’idrogeno è pari al 4% vol. Un gas di prova con il 2% volumetrico di idrogeno nell’aria non è infiammabile. Limite LEL: pericolo di esplosione. Al di sotto del limite LEL, non vi è alcun pericolo di esplosione. La limitazione delle concentrazioni e l’inertizzazione sono considerate misure primarie, perché prevengono la formazione di concentrazioni infiammabili. D’altro canto, l’uso di tipi di apparecchiature operative dotate di protezione contro le esplosioni è considerata una misura secondaria perché non impedisce la formazione di concentrazioni infiammabili, ma ne evita l’accensione. Limitare le concentrazioni significa diluirle attivamente; una misura potrebbe essere l’immissione automatica di aria fresca nelle aree pericolose non appena le concentrazioni raggiungono un limite LEL relativamente basso, ad esempio pari al 20%. Solo quando la concentrazione della sostanza continua ad aumentare (ovvero, le contromisure adottate non sono state adeguate) si dovrebbe considerare l’attivazione di misure di emergenza. Ad esempio, se si raggiunge un limite LEL pari al 40% tutte le apparecchiature operative elettriche prive di protezione contro le esplosioni dovrebbero essere arrestate. I dispositivi per la rilevazione dei gas vengono utilizzati per rilevare tali concentrazioni. L'inertizzazione rappresenta anch’essa una misura preventiva di protezione contro le esplosioni, la rilevazione dei valori di ossigeno è soggetta a requisiti specifici, almeno in Europa: anche i dispositivi di rilevazione di O2 devono essere sottoposti a prove per il tipo specifico di apparecchiature destinate a uno scopo particolare (ad es. conformità alla norma EN 50104). Figura 3 - LEL gas infiammabili [...] Gas e limite LEL In generale le sostanze al di sopra del loro punto di ebollizione sono note come gas. Pertanto, la pressione di un gas è sempre superiore alla pressione atmosferica, il che significa che, quando vengono rilasciati, i gas possono rapidamente superare il limite LEL nelle loro concentrazioni e formare miscele infiammabili di gas e aria. Vapori dei liquidi infiammabili e punto di infiammabilità Le sostanze al di sotto del loro punto di ebollizione non solo si trovano in forma gassosa, ma anche in un equilibrio specifico alle temperature nel loro stato liquido (o addirittura solido). Il componente gassoso in tali casi è noto come vapore. La pressione del vapore è sempre inferiore alla pressione atmosferica e, a seconda della temperatura, si possono formare solo determinate concentrazioni massime di vapori. In particolare, la massima pressione possibile del vapore di un liquido infiammabile può essere così bassa che il limite LEL viene raggiunto solo quando si supera una determinata temperatura, ovvero il vapore diventa infiammabile soltanto al di sopra di tale temperatura. Questa temperatura determinata empiricamente è nota come punto di infiammabilità – un valore di sicurezza estremamente importante per la valutazione del rischio rappresentato dai liquidi infiammabili. Per esempio, il punto di infiammabilità dell’etanolo puro è pari a 12 °C. Ciò significa che è combustibile già a temperature di soli 20 °C. In contrasto, il punto di infiammabilità dei vapori di n-butanolo è pari a 35 °C, e non è ancora in grado di accendersi a una temperatura di 20 °C. Temperatura di autoaccensione (accensione) ed energia minima di accensione MIE Temperatura di autoaccensione (AIT) è la temperatura più bassa (di una superficie) alla quale, in condizioni specificate (secondo IEC 6 0079-20-1), avviene l'accensione di un gas o vapore infiammabile in miscela con aria o aria/gas inerte. Tale valore è utile per determinare le massime temperature raggiungibili dalle superfici delle apparecchiature che si trovano in presenza di atmosfere potenzialmente esplosive. Le scintille prodotte elettricamente (o meccanicamente) e le superfici calde sono le più note tra i diversi tipi di sorgenti di accensione. CEI EN IEC 60079-0 3.6 auto-ignition temperature (AIT) Per accendere le miscele di gas e aria e di vapori e aria: 1. l’energia della scintilla deve superare il livello minimo di energia di accensione della miscela MIE. oppure Figura 4: Accensione di una miscela in aria: Entrambi i livelli (energia minima di accensione e temperatura di accensione) sono specifici alle sostanze, e i valori di sicurezza pertinenti sono definiti da specifiche norme di sicurezza e hanno un ruolo determinante nello sviluppo e nella selezione delle apparecchiature per la protezione contro le esplosioni. [...] Diagrammi di infiammabilità Il campo di infiammabilità di un gas sotto date condizioni di processo può essere raffigurato secondo diagrammi triangolari, come nell’esempio riportato in figura seguente (O2 / CH4 / N2): Figura 6 - Rappresentazione campo di infiammabilità di un gas [...] LOC Limiting Oxygen Concentration / MOC Minimum Oxygen Concentration Il punto C , in figura 7, rappresenta il limite della concentrazione di ossigeno al di sotto del quale nessuna miscela può essere accesa (LOC) o MOC (1). (1) LOC Limiting Oxygen Concentration / MOC Minimum Oxygen Concentration - Limite concentrazione di ossigeno in una miscela di sostanza infiammabile e aria e un gas inerte, nella quale non si verifica un'esplosione, determinata in condizioni di prova specificate. La pressione e la temperatura hanno un effetto sul diagramma di infiammabilità come riportato in figura 7, dove un incremento della pressione si traduce in un aumento del UEL ed una corrispondente diminuzione del LOC (punti C, C’, C”). Figura 8 - Effetto della pressione sul diagramma triangolare di infiammabilità relativo ad una generica miscela combustibile-ossigeno-azoto Come visto, dal diagramma di infiammabilità è possibile determinare, con semplici considerazioni geometriche, la percentuale minima di ossigeno che consente ancora la propagazione della fiamma (MOC). Altresì, nel grafico N,C (O costante) di figura 8 seguente nel campo di infiammabilità di un determinato gas è possibile determinare il MOC si considerano tutte le miscele che giacciono sulle rette parallele al lato CN del triangolo (ossidante zero) hanno un contenuto costante di ossigeno (in quanto è costante la somma inerte + combustibile). C + %Gas + %N2 = 100% %Gas = 100% - C - %N2 %Gas = K - %N2 y = K - x La retta tangente al diagramma di infiammabilità è quella che dà la concentrazione minima di ossigeno (MOC). Al di sotto del valore critico dell'ossigeno minimo, nessuna miscela combustibile-aria-diluente risulta infiammabile. Figura 9 - Determinazione grafica dell'ossigeno minimo (MOC) Note sui Diagrammi ternari Una miscela a tre componenti può essere rappresentata con un diagramma ternario formato da un triangolo equilatero. Si pone uguale a 100 il lato del triangolo e si sfruttano le sue proprietà: osservando la figura, si vede facilmente che preso un qualsiasi punto P interno al triangolo, la somma a + b + c = AB = AC = BC; infatti (lato sinistro), BA = BT + TA = (a + c) + b. Questo significa che la composizione di una qualsiasi miscela, interna al triangolo ha somma costante. Le letture delle singole percentuali si fanno sempre intersecando in P (punto del quale si vuole conoscere la composizione) le tre parallele ai lati ed eseguendo la lettura dei segmenti a, b, c. Figura 10 - Diagramma triangolare (ternario) Figura 11 – Diagramma triangolare O2 / N2 / CH4 Per il punto P e in qualsia punto del diagramma, risulta che le concentrazioni di O2 / N2 / CH4 rispettano l’equazione (T 25° / P atmosferica): PO2 + PN2 + PCH4 = 100% Osservando il diagramma seguente Figura 10, in combinazione con la tabella 1, si può verificare la capacità di leggere correttamente un diagramma triangolare. Tabella 1 - Tabella concentrazioni di esempio Figura 12 - Lettura diagramma triangolare Punti P1, P2, P3, P4 [...] Aggiunta di inerti L'intervallo di infiammabilità di una sostanza infiammabile con l'aria è sempre meno esteso di quello dello stesso infiammabile con il solo ossigeno, in quanto l'azoto presente nell'aria (circa il 79%) non reagisce chimicamente nella combustione ed è dunque da considerarsi un diluente che diminuisce l'infiammabilità della miscela. La presenza di gas inerti (N2, CO2, ecc.) abbassa notevolmente il limite superiore di esplodibilità UEL del combustibile, senza far variare sensibilmente quello inferiore LEL. Figura 13 - Riduzione UEL In tal modo il campo di infiammabilità si restringe sempre più; continuando nell'aggiunta dell’inerte fino a che i due limiti praticamente coincidono si determina la "penisola di infiammabilità" entro la quale tutti i punti corrispondono a miscele infiammabili; al di fuori, tutti i punti corrispondono a miscele non infiammabili. Tabella 2 - Effetto di diversi gas inerti sull'infiammabilità del metano ... Certifico Srl - IT | Rev. 0.0 2023 Matrice revisioni
Info e download
|
|||||||||
 |
|||||||||
|
è un sito di INVIO NEWSLETTTER Se vuoi cancellarti dall'invio della newsletter oppure effettua il login al sito ed entra nella Tua Area Riservata, in “Modifica dati” agisci con la spunta sul box di selezione “Newsletter”. L'Elenco completo di tutte le ns newsletter è qui: Archivio newletter |
|||||||||
  |
|||||||||
| Certifico Srl 2000-2025 | VAT IT02442650541 | |||||||||