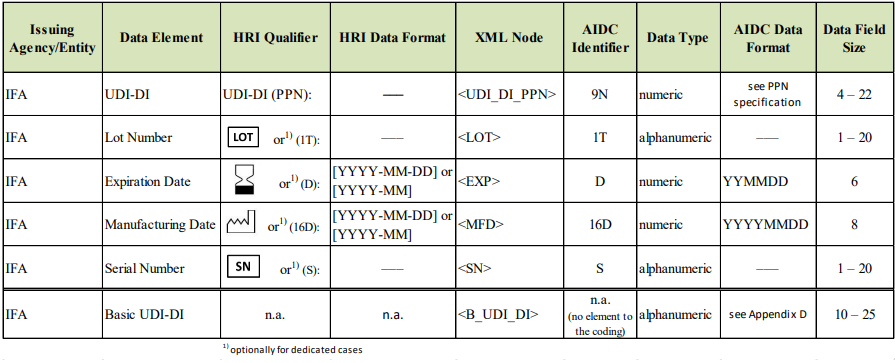
IFA Standards
The Basic UDI-DI is generated from these four elements (substring elements):
- Issuing Agency Code (IAC)
- Manufacturer Code
- Device Group Code
- Check Digit
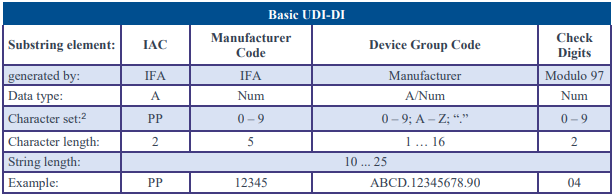
From the example shown in the table and from the sequence of the four elements (without additional delimiters) results the Basic UDI-DI: “PP12345ABCD.12345678.9004“.
Supplementary information:
IAC: The code “PP” must always be used as the IAC assigned to IFA as the issuing agency.
Manufacturer Code: Here, the manufacturer uses the five-digit IFA supplier number assigned by IFA. It can be found in the overview of supplier address data, which can be requested from IFA.
Device Group Code: This code for the product group in question is assigned by the manufacturer in consideration of the rules stipulated by the Commission. At the time these specifications were generated, the guideline “MDCG 2018-1 v2 Guidance on BASIC UDI-DI and changes to UDI-DI” applied.
For any division within the substring “Device Group Code”, the period “.” can be used.
Check Digits: The check digits in two-digit format are formed via the first three substrings. Here, the method in accordance with Modulo 97 is used in identical form, as for the calculation of the check digits of the PPN. The procedure is described in the IFA document Technical Information – Check Digit Calculations