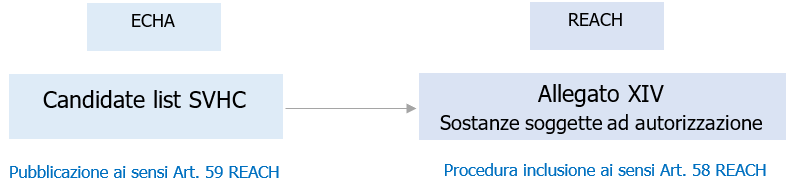
Regolamento 1907/2006 (REACH): Artt. 57, 58, 59
...
Articolo 57 Sostanze da includere nell'allegato XIV Le sostanze seguenti possono essere incluse nell'allegato XIV secondo la procedura di cui all'articolo 58:
a) le sostanze che rispondono ai criteri di classificazione nella classe di pericolo cancerogenicità, categoria 1A o 1B, di cui al punto 3.6 dell'allegato I del
regolamento (CE) n. 1272/2008;
b) le sostanze che rispondono ai criteri di classificazione nella classe di pericolo mutagenicità sulle cellule germinali, categoria 1A o 1B, di cui al punto 3.5 dell'allegato I del
regolamento (CE) n. 1272/2008;
c) le sostanze che rispondono ai criteri di classificazione nella classe di pericolo tossicità per la riproduzione, categoria 1A o 1B, effetti nocivi sulla funzione sessuale e la fertilità o sullo sviluppo di cui al punto 3.7 dell'allegato I del
regolamento (CE) n. 1272/2008;
d) le sostanze che sono persistenti, bioaccumulabili e tossiche, secondo i criteri di cui all'allegato XIII del presente regolamento;
e) le sostanze che sono molto persistenti e molto bioaccumulabili, secondo i criteri di cui all'allegato XIII del presente regolamento;
f) le sostanze come quelle aventi proprietà che perturbano il sistema endocrino o quelle aventi proprietà persistenti, bioaccumulabili e tossiche o molto persistenti e molto bioaccumulabili, che non rispondono ai criteri di cui alle lettere d) o e), per le quali è scientificamente comprovata la probabilità di effetti gravi per la salute umana o per l'ambiente che danno adito ad un livello di preoccupazione equivalente a quella suscitata dalle altre sostanze di cui alle lettere da a) a e), e che sono identificate in base ad una valutazione caso per caso secondo la procedura di cui all'articolo 59.
Articolo 58 Inclusione di sostanze nell'allegato XIV 1. Ogniqualvolta si decide di includere nell'allegato XIV una o più sostanze di cui all'articolo 57, la decisione è assunta secondo la procedura di cui all'articolo 133, paragrafo 4. Per ogni sostanza, è precisato quanto segue:
a) l'identità della sostanza, come specificato nell'allegato VI, punto 2;
b) la o le proprietà intrinseche della sostanza di cui all'articolo 57;
c) disposizioni transitorie:
i) la data o le date a partire dalle quali l'immissione sul mercato e l'uso della sostanza sono vietati, salvo qualora sia rilasciata un'autorizzazione (in seguito denominata: «data di scadenza»), che dovrebbero tener conto, se del caso, del ciclo di produzione specificato per tale uso;
ii) una o più date precedenti di almeno diciotto mesi la o le date di scadenza, entro cui devono pervenire le domande se il richiedente intende continuare a utilizzare la sostanza o a immetterla sul mercato per determinati usi dopo la o le date di scadenza; la prosecuzione di tali usi è autorizzata dopo la data di scadenza fintantoché non è assunta una decisione sulla domanda di autorizzazione;
d) se del caso, i periodi di revisione per taluni usi; e) gli eventuali usi o categorie di usi esentati dall'obbligo d'autorizzazione e le eventuali condizioni di tali esenzioni.
2. Gli usi o categorie di usi possono essere esentati dall'obbligo di autorizzazione, a condizione che il rischio sia adeguatamente controllato, in base alla vigente normativa comunitaria specifica che impone prescrizioni minime per l'uso della sostanza connesse alla protezione della salute umana o alla tutela dell'ambiente. Nello stabilire tali esenzioni, si tiene conto, in particolare, della proporzionalità del rischio per la salute umana e per l'ambiente connessa alla natura della sostanza, come nel caso in cui il rischio è modificato dalla forma fisica.
3. Prima di assumere una decisione sull'inclusione di sostanze nell'allegato XIV, l'Agenzia, tenuto conto del parere del comitato degli Stati membri, raccomanda sostanze prioritarie da includere, precisando per ogni sostanza gli elementi di cui al paragrafo 1. Di norma, sono considerate prioritarie le sostanze:
a) che hanno proprietà PBT o vPvB; o
b) il cui uso è fortemente dispersivo; o
c) che sono prodotte ad alti volumi.
Il numero di sostanze incluse nell'allegato XIV e le date fissate a norma del paragrafo 1 tengono conto anche della capacità dell'Agenzia di evadere le domande nei termini previsti. L'Agenzia redige la prima raccomandazione relativa a sostanze prioritarie da includere nell'allegato XIV entro il 1o giugno 2009. L'Agenzia redige ulteriori raccomandazioni, quantomeno ogni due anni, nell'ottica di includere altre sostanze nell'allegato XIV.
4. Prima di trasmetterla alla Commissione, l'Agenzia pubblica la raccomandazione sul suo sito web, indicando chiaramente la data di pubblicazione, nel rispetto delle disposizioni degli articoli 118 e 119 sull'accesso alle informazioni. Essa invita tutte le parti interessate a presentare, entro i tre mesi successivi alla data di pubblicazione, osservazioni riguardanti in particolare gli usi che dovrebbero essere esentati dall'obbligo d'autorizzazione. L'Agenzia aggiorna la sua raccomandazione tenendo conto delle osservazioni ricevute.
5. Fatto salvo il paragrafo 6, una volta inclusa nell'allegato XIV, una sostanza non è assoggettata a nuove restrizioni secondo la procedura di cui al titolo VIII in relazione ai rischi che l'uso della sostanza in quanto tale, come componente di una miscela o incorporata in un articolo, comporta per la salute umana o per l'ambiente a motivo delle proprietà intrinseche di cui all'allegato XIV.
6. Una sostanza elencata nell'allegato XIV può essere assoggettata a nuove restrizioni secondo la procedura di cui al titolo VIII in relazione ai rischi che la presenza della sostanza in uno o più articoli comporta per la salute umana o per l'ambiente.
7. Le sostanze per le quali sono stati vietati tutti gli usi a norma del titolo VIII o di altre normative comunitarie non sono incluse nell'allegato XIV o ne sono depennate.
8. Le sostanze che in base a nuove informazioni non risultano più rispondere ai criteri di cui all'articolo 57, sono depennate dall'allegato XIV secondo la procedura di cui all'articolo 133, paragrafo 4.
Articolo 59 Identificazione delle sostanze di cui all'articolo 57
1. Ai fini dell'identificazione delle sostanze che rispondono ai criteri di cui all'articolo 57 e della definizione di un elenco di sostanze candidate all'eventuale inclusione nell'allegato XIV, si applica la procedura di cui ai paragrafi da 2 a 10 del presente articolo. L'Agenzia indica, in questo elenco, le sostanze che figurano nel programma di lavoro di cui all'articolo 83, paragrafo 3, lettera e).
2. La Commissione può chiedere all'Agenzia di predisporre un fascicolo, a norma dei pertinenti punti dell'allegato XV, per le sostanze che, a suo giudizio, rispondono ai criteri di cui all'articolo 57. Il fascicolo può essere limitato, se del caso, a un riferimento a una voce dell'allegato VI, parte 3, del regolamento (CE) n. 1272/2008.; L'Agenzia mette il fascicolo a disposizione degli Stati membri.
3. Ogni Stato membro può predisporre un fascicolo a norma dell'allegato XV per le sostanze che, a suo giudizio, rispondono ai criteri di cui all'articolo 57 e trasmetterlo all'Agenzia. Il fascicolo può essere limitato, se del caso, a un riferimento a una voce dell'allegato VI, parte 3, del regolamento (CE) n. 1272/2008. L'Agenzia mette il fascicolo a disposizione degli altri Stati membri entro trenta giorni dalla ricezione.
4. L'Agenzia pubblica sul suo sito web un avviso dell'avvenuta predisposizione a norma dell'allegato XV di un fascicolo per una sostanza. L'Agenzia invita tutte le parti interessate a trasmetterle osservazioni entro un termine stabilito.
5. Entro sessanta giorni dalla messa a disposizione, gli altri Stati membri o l'Agenzia possono formulare osservazioni sull'identificazione della sostanza in relazione ai criteri di cui all'articolo 57 nel fascicolo trasmesso all'Agenzia.
6. Se non riceve o non formula osservazioni, l'Agenzia può includere la sostanza nell'elenco di cui al paragrafo 1. Essa può includere la sostanza nelle raccomandazioni che formula a norma dell'articolo 58, paragrafo 3.
7. Qualora vengano formulate o ricevute osservazioni, l'Agenzia rinvia il fascicolo al comitato degli Stati membri entro quindici giorni dallo scadere del periodo di sessanta giorni di cui al paragrafo 5.
8. Se, entro trenta giorni da tale rinvio, il comitato degli Stati membri giunge ad un accordo unanime sull'identificazione, l'Agenzia include la sostanza nell'elenco di cui al paragrafo 1. Essa può includere tale sostanza nelle raccomandazioni che formula a norma dell'articolo 58, paragrafo 3.
9. Se il comitato degli Stati membri non riesce a giungere a un accordo unanime, entro tre mesi dalla ricezione del parere del comitato degli Stati membri la Commissione prepara un progetto di proposta relativa all'identificazione della sostanza in questione. La decisione definitiva sull'identificazione della sostanza è assunta secondo la procedura di cui all'articolo 133, paragrafo 3.
10. Non appena è stata assunta una decisione sull'inclusione di una sostanza l'Agenzia pubblica e aggiorna senza indugio sul suo sito web l'elenco di cui al paragrafo 1.