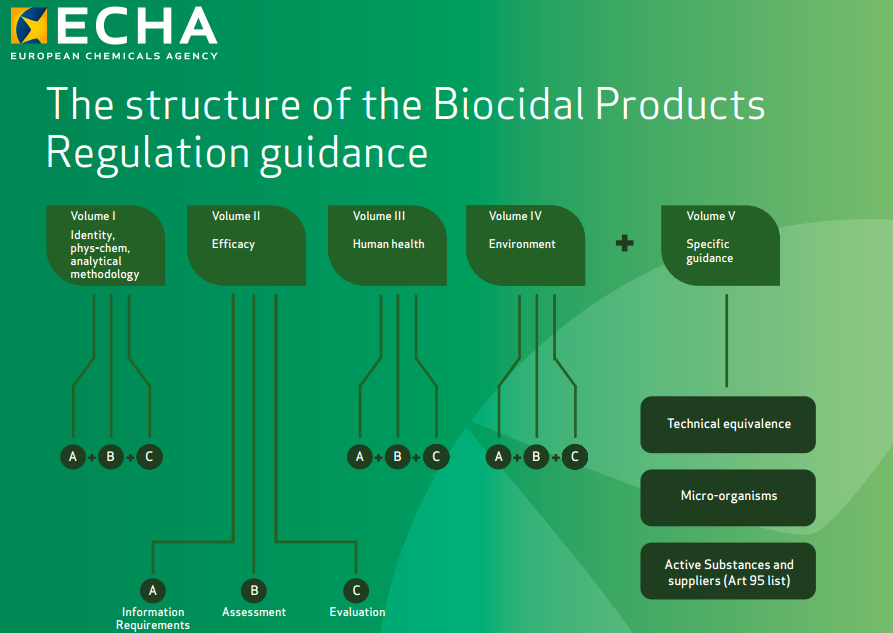
The structure of the Biocidal Products Regulation guidance
Allegati tutti i documenti d'orientamento che sono disponibili sul sito ECHA. relativi ai biocidi, Regolamento (UE) 528/2012 (BPR)
Il regolamento sui biocidi (BPR, regolamento (UE) 528/2012) concerne l'immissione sul mercato e l'uso di biocidi, utilizzati per la tutela dell'uomo, degli animali, dei materiali o degli articoli contro organismi nocivi, quali parassiti o batteri, mediante l'azione dei principi attivi contenuti nel biocida. Lo scopo del regolamento è migliorare il funzionamento del mercato dei biocidi nell'UE, garantendo allo stesso tempo un elevato livello di tutela per l'uomo e per l'ambiente.
Il testo è stato adottato il 22 maggio 2012 e trovato applicazione a partire dal 1º settembre 2013, con un periodo di transizione per determinate disposizioni. Il regolamento abroga la direttiva sui biocidi (direttiva 98/8/CE).
Tutti i biocidi necessitano di un'autorizzazione prima di poter essere immessi sul mercato; inoltre, i principi attivi in essi contenuti devono essere stati precedentemente approvati. Esistono, tuttavia, alcune eccezioni a tale prassi. Ad esempio, i biocidi contenenti principi attivi soggetti al programma di riesame possono essere resi disponibili sul mercato e utilizzati (nel rispetto delle normative nazionali) in attesa della decisione finale sull'approvazione del principio attivo (e fino a tre anni dopo). Inoltre, anche i prodotti contenenti nuovi principi attivi ancora in fase di valutazione possono essere immessi sul mercato sulla base di autorizzazioni provvisorie.
Il BPR si pone come obiettivo di armonizzare il mercato a livello dell'Unione, di semplificare l'approvazione dei principi attivi e l'autorizzazione dei biocidi e di introdurre scadenze per le valutazioni, l'elaborazione di pareri e la formulazione di decisioni a livello degli Stati membri. Promuove inoltre la riduzione delle sperimentazioni sugli animali, introducendo obblighi relativi alla condivisione dei dati e incoraggiando l'uso di metodi di sperimentazione alternativi.
Come nella precedente direttiva, l'approvazione dei principi attivi avviene a livello dell'Unione e la successiva autorizzazione dei biocidi a livello degli Stati membri. Tale autorizzazione può essere estesa ad altri Stati membri tramite riconoscimento reciproco. Tuttavia, il nuovo regolamento fornisce ai richiedenti anche la possibilità di ottenere un nuovo tipo di autorizzazione a livello dell'Unione (autorizzazione dell'Unione).
Allegati tutti i documenti d'orientamento che sono o saranno disponibili sul sito ECHA.
Tali documenti sono stati elaborati con la partecipazione di Stati membri, industria e parti interessate accreditate. L'obiettivo dei documenti è agevolare l'attuazione del regolamento relativo ai biocidi (BPR) descrivendo le buone pratiche su come soddisfare gli obblighi.
Oltre all'orientamento sul BPR, l'orientamento sulla direttiva relativa ai biocidi (BPD) e altri documenti correlati sono considerati applicabili per le nuove presentazioni a norma del BPR nei settori per i quali l'orientamento sul BPR è ancora in fase di preparazione. Inoltre questi documenti sono ancora validi in relazione alle domande per l'iscrizione dei principi attivi nell'allegato I o alle domande di autorizzazione di un prodotto a norma del BPD che possono essere ancora in corso di valutazione.
Volume I - Identity, phys-chem, analytical methodology
Volume II - Efficacy
Volume III - Human health Volume
IV - Environment Volume
V - Specific guidance
ECHA Update Febb. 2017
Allegati
|
Descrizione |
Lingua |
Dimensioni |
Downloads |
 |
|
EN |
1205 kB |
306 |
 |
|
EN |
311 kB |
299 |
 |
|
EN |
342 kB |
282 |
 |
|
EN |
885 kB |
318 |
 |
|
EN |
3776 kB |
423 |
 |
|
EN |
1480 kB |
309 |
 |
|
EN |
4599 kB |
364 |
 |
|
EN |
1010 kB |
281 |
 |
|
EN |
735 kB |
318 |
 |
|
EN |
1397 kB |
334 |


































